Selluloosa
| Selluloosa | |
|---|---|
| | |
| Kenraali | |
| Chem. kaava | ( C6H10O5 ) n _ _ _ _ |
| Fyysiset ominaisuudet | |
| Osavaltio | valkoinen jauhe |
| Moolimassa | 162,1406 massa glukoosimonomeeriä g/ mol |
| Tiheys | ~1,5 g/cm³ |
| Lämpöominaisuudet | |
| Lämpötila | |
| • sulaminen | 467 °C |
| • hajoaminen | 260±1 ja 270±1 °C |
| Höyryn paine | 0 ± 1 mmHg [yksi] |
| Luokitus | |
| Reg. CAS-numero | 9004-34-6 |
| Reg. EINECS-numero | 232-674-9 |
| Codex Alimentarius | E460 |
| RTECS | FJ5691460 |
| CHEBI | 18246 |
| Turvallisuus | |
| NFPA 704 |
 yksi
yksi
0
yksi
yksi
0 |
| Tiedot perustuvat standardiolosuhteisiin (25 °C, 100 kPa), ellei toisin mainita. | |
| Mediatiedostot Wikimedia Commonsissa | |
Selluloosa , kuitu ( fr. selluloosa lat. sellulasta - " solu ") - orgaaninen yhdiste , hiilihydraatti , polysakkaridi , jonka kaava on (C 6 H 10 O 5 ) n . Molekyylit ovat haaroittumattomia β - glukoositähteiden ketjuja, jotka on yhdistetty β-(1→4) -glykosidisidoksilla . Valkoinen kiinteä aine, veteen liukenematon. Kaikkien korkeampien kasvien solukalvojen pääkomponentti .
Historia
Ranskalainen kemisti Anselme Payen löysi ja kuvasi selluloosan vuonna 1838. [2]
Rakennus
Selluloosa on lineaarinen homopolymeeri , jossa on satoja tai kymmeniä tuhansia D-glukoosijäämiä . Glukoosifragmenttien yhteys saadaan aikaan β (1→4) - glykosidisidoksella . Tällainen monomeeriyksiköiden kytkentä erottaa selluloosan α (1 → 4)-glykosidisidoksista, jotka ovat ominaisia muille glukoosihomopolymeereille: tärkkelykselle ja glykogeenille . Toisin kuin tärkkelysamyloosi , jonka molekyylit ovat kierrettyjä, selluloosan makromolekyylillä on taipumus saada pitkänomainen sauvarakenne.
Fysikaaliset ominaisuudet
Selluloosa on valkoinen kiinteä, stabiili aine, joka ei hajoa kuumennettaessa (200 °C asti). Se on palava aine, hajoamislämpötila on 275 °C [3] , itsesyttymislämpötila on 420 °C (puuvillaselluloosa). Vuonna 2016 selluloosan sulaminen 467 °C:ssa osoitettiin kokeellisesti [4] .
Liukenematon veteen, heikkoihin happoihin ja useimpiin orgaanisiin liuottimiin. Hydroksyyliryhmien suuren määrän vuoksi se on kuitenkin hydrofiilinen ( kosketuskulma on 20-30 astetta) [5] .
Selluloosalla ei ole makua tai hajua. Rekisteröity elintarvikelisäaineeksi E460.
Selluloosa hajoaa biologisesti monien mikro -organismien mukana .
Kemialliset ominaisuudet
Selluloosa koostuu glukoosimolekyylien jäämistä , joita muodostuu selluloosan hydrolyysin aikana:
(C 6 H 10 O 5 ) n + n H 2 O → n C 6 H 12 O 6Rikkihappo jodin kanssa , hydrolyysin seurauksena , väri selluloosansiniseksi.
Kun reagoidaan typpihapon kanssa , muodostuu nitroselluloosaa ( selluloosatrinitraattia ):
Selluloosan esteröiminen etikkahapolla tuottaa selluloosatriasetaattia : _
Selluloosa on äärimmäisen vaikeasti liukenevaa ja kemiallisia lisämuutoksia, mutta sopivassa liuotinympäristössä, esimerkiksi ionisessa nesteessä , tällainen prosessi voidaan suorittaa tehokkaasti [6] .
Haetaan
Sellua saadaan teollisella menetelmällä keittämällä haketta sellutehtailla, jotka ovat osa teollisuuskomplekseja ( kombinaatteja ). Käytettyjen reagenssien tyypin mukaan erotetaan seuraavat massanvalmistusmenetelmät:
- hapan :
- Sulfiitti . Keittoliuos sisältää rikkihappoa ja sen suolaa, esimerkiksi natriumhydrosulfiittia . Tätä menetelmää käytetään selluloosan saamiseksi vähän hartsipitoisista puulajeista : kuusesta, kuusesta.
- Alkalinen :
- Natronny . Käytetään natriumhydroksidiliuosta . Soodamenetelmällä voidaan saada selluloosaa lehtipuista ja yksivuotisista kasveista. Tämän menetelmän etuna on rikkiyhdisteiden epämiellyttävän hajun puuttuminen, haittoja ovat saadun selluloosan korkeat kustannukset.
- sulfaatti . Yleisin menetelmä nykyään. Natriumhydroksidia ja natriumsulfidia sisältävää liuosta, ja sitä kutsutaan valkolipeäksi . Menetelmä on saanut nimensä natriumsulfaatista , josta sellutehtailla saadaan valkolipeän sulfidia. Menetelmä soveltuu selluloosan saamiseen mistä tahansa kasvimateriaalista. Sen haittana on, että sivureaktioiden seurauksenavapautuu suuri määrä pahanhajuisia rikkiyhdisteitä: metyylimerkaptaania , dimetyylisulfidia jne.
Kypsennyksen jälkeen saatu tekninen selluloosa sisältää erilaisia epäpuhtauksia: ligniiniä , hemiselluloosia . Jos selluloosa on tarkoitettu kemialliseen käsittelyyn (esimerkiksi keinokuitujen valmistukseen), se puhdistetaan - käsitellään kylmällä tai kuumalla alkaliliuoksella hemiselluloosien poistamiseksi .
Jäännösligniinin poistamiseksi ja massan valkaisemiseksi se valkaistaan. 1900-luvulla perinteinen kloorivalkaisu sisälsi kaksi vaihetta:
- kloorikäsittely - ligniinimakromolekyylien tuhoamiseen;
- alkalikäsittely - muodostuneiden ligniinin tuhoamistuotteiden uuttamiseen.
Otsonivalkaisua on myös alettu käyttää 1970-luvulta lähtien. 1980-luvun alussa ilmestyi tietoa erittäin vaarallisten aineiden - dioksiinien - muodostumisesta kloorivalkaisuprosessissa . Tämä johti tarpeeseen korvata kloori muilla reagensseilla. Tällä hetkellä valkaisutekniikat jaetaan:
- ECF (Elemental chlorine free) - ilman alkuaineklooria, korvaamalla sen klooridioksidilla .
- TCF (Total chlorine free) – täysin klooriton valkaisu. Käytetään happea , otsonia , vetyperoksidia ja paljon muuta .
Sovellus
Käytetään farmaseuttisten tablettien täyteaineena. Selluloosaa ja sen estereitä käytetään tekokuitujen valmistukseen ( viskoosi , asetaatti , kupari-ammoniakkisilkki , tekoturkikset ). Puuvillaa , joka koostuu pääosin selluloosasta (jopa 99,5 %), käytetään kankaiden valmistukseen .
Puumassasta valmistetaan paperia , muoveja , filmejä ja valokuvafilmejä , lakkoja , savutonta jauhetta jne. [7]
Luonnossa oleminen
Selluloosa on yksi kasvien soluseinien pääkomponenteista , vaikka sen pitoisuus eri soluissa tai jopa saman soluseinän osissa vaihtelee suuresti. Joten esimerkiksi viljan endospermin soluseinämät sisältävät vain noin 2 % selluloosaa, kun taas puuvillansiemeniä ympäröivät puuvillakuidut koostuvat yli 90 % selluloosasta. Polaarisen kasvun omaavien pitkänomaisten solujen kärjen alueella olevat soluseinät ( siitepölyputki , juurikarvat ) eivät sisällä käytännössä lainkaan selluloosaa ja koostuvat pääasiassa pektiinistä , kun taas näiden solujen tyviosat sisältävät merkittäviä määriä selluloosaa. Lisäksi selluloosan pitoisuus soluseinässä muuttuu ontogeneaation aikana , yleensä sekundääriset soluseinät sisältävät enemmän selluloosaa kuin primääriset.
Organisaatio ja toiminta soluseinissä
Yksittäiset selluloosamakromolekyylit sisältävät 2 - 25 tuhatta D-glukoositähdettä. Soluseinissä oleva selluloosa on organisoitunut mikrofibrilleiksi, jotka ovat parakiteisiä ryhmiä useista erillisistä makromolekyyleistä ( noin 36 vaskulaarisissa kasveissa ) [8] , jotka liittyvät toisiinsa vetysidoksilla ja van der Waalsin voimilla .
Samassa tasossa sijaitsevat ja vetysidoksilla toisiinsa yhdistetyt makromolekyylit muodostavat levyn mikrofibrilliin. Makromolekyylien levyt ovat myös yhteydessä toisiinsa suurella määrällä vetysidoksia. Vaikka vetysidokset ovat melko heikkoja, niiden runsauden vuoksi selluloosamikrofibrillillä on korkea mekaaninen lujuus ja entsyymitoiminnan kestävyys .
Mikrofibrillissä olevat yksittäiset makromolekyylit alkavat ja päättyvät eri paikoissa, joten mikrofibrillien pituus ylittää yksittäisten selluloosamakromolekyylien pituuden. On huomattava, että mikrofibrillissä olevat makromolekyylit ovat samalla tavalla orientoituneita, eli pelkistävät päät (päät, joissa on vapaa, anomeerinen OH-ryhmä C1- atomissa ) sijaitsevat toisella puolella.
Nykyaikaiset selluloosamikrofibrillien järjestäytymismallit viittaavat siihen, että sillä on erittäin organisoitunut rakenne keskialueella ja makromolekyylien järjestely muuttuu kaoottisemmaksi reunaa kohti. Joten korkeampien kasvien mikrofibrillien keskellä on 24 molekyylin ydin. Toiset 12 molekyyliä sijaitsevat fibrillin reunalla. Teoreettisesti tällaisen mikrofibrillin halkaisija on 3,8 nm, mutta röntgendiffraktioanalyysitiedot osoittavat, että tämä arvo on hieman pienempi - 3,3 nm, mikä vastaa 24 molekyyliä. [8] Muiden arvioiden mukaan fibrillien koot ovat paljon suurempia: 5–9 nm poikkileikkaukseltaan (yli 50 yksittäistä makromolekyyliä). [9]
Mikrofibrillit ovat yhteydessä toisiinsa silloittavilla glykaaneilla ( hemiselluloosalla ) ja vähemmässä määrin pektiinillä . Selluloosa mikrofibrillit, jotka on yhdistetty silloittuvilla glykaaneilla, muodostavat kolmiulotteisen verkoston, joka on upotettu geelimäiseen pektiinimatriisiin ja tarjoavat korkean lujuuden soluseinämille.
Toissijaisissa soluseinissä mikrofibrillit voivat liittyä nipuiksi, joita kutsutaan makrofibrilleiksi. Tämä organisaatio lisää edelleen soluseinän lujuutta.
Biosynteesi
Selluloosamakromolekyylien muodostumista korkeampien kasvien soluseinissä katalysoi monialayksikkömembraaniselluloosasyntaasikompleksi, joka sijaitsee pidentyvien mikrofibrillien päässä. Täydellinen selluloosasyntaasikompleksi koostuu katalyyttisistä, huokos- ja kiteytysalayksiköistä. Selluloosasyntaasin katalyyttistä alayksikköä koodaa CesA ( selluloosasyntaasi A ) -monigeeniperhe, joka on Csl -superperheen ( selluloosasyntaasin kaltainen ) jäsen, joka sisältää myös CslA- , CslF- , CslH- ja CslC-geenit . muiden polysakkaridien synteesi.
Tutkittaessa kasvisolujen plasmalemman pintaa jäädyttämällä pilkkomalla selluloosamikrofibrillien tyvestä voidaan havaita ns. ruusukkeita tai terminaalikomplekseja, joiden koko on noin 30 nm ja jotka koostuvat 6 alayksiköstä. Jokainen tällainen ruusukkeen alayksikkö on vuorostaan superkompleksi, joka muodostuu kuudesta selluloosasyntaasista. Siten tällaisen ruusukkeen toiminnan seurauksena muodostuu mikrofibrilli, joka sisältää noin 36 selluloosamakromolekyyliä poikkileikkaukseltaan. Joissakin levissä selluloosasynteesin superkompleksit ovat lineaarisesti järjestäytyneitä.
Mielenkiintoista on, että glykosyloitu sitosteroli toimii siemenenä selluloosasynteesin käynnistämisessä . Selluloosasynteesin suora substraatti on UDP-glukoosi. Selluloosasyntaasiin liittyvä sakkaroosisyntaasi on vastuussa UDP-glukoosin muodostumisesta ja suorittaa reaktion:
Sakkaroosi + UDP UDP-glukoosi + D-fruktoosiLisäksi UDP-glukoosi voi muodostua heksoosifosfaattipoolista UDP-glukoosipyrofosforylaasin työn tuloksena:
Glukoosi-1-fosfaatti + UTP UDP-glukoosi + PP iSelluloosamikrofibrillien synteesin suunta saadaan aikaan selluloosasyntaasikompleksien liikkeellä plasmalemman vieressä olevia mikrotubuluksia pitkin sisältäpäin. Talyan apilan mallikasvista löydettiin CSI1-proteiini, joka on vastuussa selluloosasyntaasikompleksien kiinnittymisestä ja liikkumisesta aivokuoren mikrotubuluksia pitkin .
Jakaminen
Nisäkkäillä ( kuten useimmilla muilla eläimillä) ei ole entsyymejä , jotka voivat hajottaa selluloosaa. Kuitenkin monien kasvinsyöjien (kuten märehtijöiden ) ruoansulatuskanavassa on symbionttibakteereja, jotka hajoavat ja auttavat isäntiään imemään tätä polysakkaridia. Selluloosan hajoaminen liittyy sellulaasientsyymin toimintaan hajoavissa organismeissa . Selluloosaa hajottavat bakteerit, joita kutsutaan sellulolyyttisiksi bakteereiksi , ovat usein Cellulomonas -suvun aktinobakteereja , jotka ovat fakultatiivisia anaerobeja [10] [11] , Cellvibrio -suvun aerobisia bakteereja [ 12] . Kuitenkin esimerkiksi paperikirjoille ne ovat vaarallisia vain kastuessaan, kun ihoa ja liimaa alkavat tuhota mädäntymisbakteerit ja paperia ja kankaita - selluloosaa tuhoamalla [13] . Selluloosaa tuhoavat muotit ovat erittäin vaarallisia paperikirjoille . Kolmessa kuukaudessa ne voivat tuhota 10-60 % paperikuiduista, suotuisia olosuhteita niiden kehittymiselle ovat kosteus ja kostea ilma , suotuisin lämpötila on +22 - +27 celsiusastetta, ne voivat levitä kirjoista, joihin ne vaikuttavat. muille [13] . Selluloosaa aktiivisesti hajottavia homeita ovat esimerkiksi Chaetomium globosum , Stachybotrys echinata [14] .
Katso myös
- Luettelo sellua tuottavista maista
- sulfaattiprosessi
- selluloosa-asetaatti
- Anselm Paya
- Airlaid (selluloosakuitukangas)
Muistiinpanot
- ↑ http://www.cdc.gov/niosh/npg/npgd0110.html
- ↑ Nikitin N.I. Puun ja sellun kemia . - M . : Nauka (kustantaja) , 1962. - S. 427. - 713 s.
- ↑ Gagić T. , Perva-Uzunalić A. , Knez Ž. , Škerget M. Selluloosan hydroterminen hajoaminen lämpötilassa 200 - 300 °C (englanniksi) // Industrial & Engineering Chemistry Research. - 2018. - Vol. 57 , no. 18 . - P. 6576-6584 . — ISSN 0888-5885 . - doi : 10.1021/acs.iecr.8b00332 .
- ↑ Dauenhauer P., Krumm C., Pfaendtner J. Millisekunnin pulssikalvot yhdistävät selluloosan pirstoutumisen mekanismeja // Materiaalien kemia. - 2016. - Vol. 28 , ei. 1 . — P. 0001 . - doi : 10.1021/acs.chemmater.6b00580 .
- ↑ Bishop CA Tyhjiöpinnoitus rainoille, kalvoille ja kalvoille . - 2007. - s. 165. - ISBN 0-8155-1535-9 .
- ↑ Ignatyev I. et ai. Glukoosiestereiden synteesi selluloosasta ionisissa nesteissä (englanniksi) // Holzforschung. - 2011. - Vol. 66 , nro. 4 . - s. 417-425 . - doi : 10.1515/hf.2011.161 .
- ↑ Glinka N. L. Yleinen kemia. - 22 painos, Rev. - Leningrad: Kemia, 1977. - 719 s.
- ↑ 1 2 Kasvien biokemia ja molekyylibiologia . - Toinen painos. - Chichester, West Sussex. — xv, 1264 sivua s. — ISBN 9780470714225 .
- ↑ Nobel, Park S. Fysikaalis-kemiallinen ja ympäristökasvien fysiologia . – 4. painos - Amsterdam: Academic Press, 2009. - 1 online-lähde (xxi, 582 sivua) s. — ISBN 9780123741431 .
- ↑ Melissa R. Christopherson, et ai. Cellulomonas fimin ja "Cellvibrio gilvuksen" genomisekvenssit paljastavat kahden fakultatiivisen anaerobin sellulolyyttiset strategiat, "Cellvibrio gilvuksen" siirtymisen Cellulomonas-sukuun ja ehdotuksen Cellulomonas gilvus sp. marraskuu (eng.) : päiväkirja. - 2013. - doi : 10.1371/journal.pone.0053954 .
- ↑ Muhammad Irfan et ai. Sellulolyyttisten bakteerien eristäminen ja seulonta maaperästä ja sellulaasituotannon ja -aktiivisuuden optimointi (englanniksi) // Turkish Journal of Biochemistry : Journal. - 2012. - Vol. 37 , no. 3 . - s. 287-293 . - doi : 10.5505/tjb.2012.09709 .
- ↑ Don J. Brenner, Noel R. Krieg, James R. Staley. Osa B: Gammaproteobakteerit // Bergeyn Systematic Bacteriology Manual (bulgaria) . - Springer Science & Business Media , 2007. - V. 2. The Proteobacteria. - S. 402-403.
- ↑ 1 2 I. K. Belaya. Kirjaston kokoelmien hygienia ja entisöinti . - Ripol Classic, 2013. - S. 13-21.
- ↑ Brian Flannigan, Robert A. Samson, J. David Miller. Mikro-organismit koti- ja sisätyöympäristöissä: monimuotoisuus, terveysvaikutukset, tutkiminen ja valvonta . – 2. painos - CRC Press , 2016. - s. 77.
Linkit
- Artikkeli "Selluloosa" (Chemical Encyclopedia)
- LSBU selluloosasivu
- Selkeä kuvaus selluloosamääritysmenetelmästä USDA : n Cotton Fiber Biosciences -yksikössä
- Selluloosa Etanolin tuotanto - Ensimmäinen kaupallinen tehdas
| | |
|---|---|
| Sanakirjat ja tietosanakirjat |
|
| Bibliografisissa luetteloissa |
| Multisakkaridit | |
|---|---|
| disakkarideja |
|
| Trisakkaridit |
|
| Tetrasakkaridit | |
| Pentasakkaridit |
|
| Heksasakkaridit |
|
| Oligosakkaridit |
|
| Polysakkaridit | |
| kasvisolu | |||||
|---|---|---|---|---|---|
| Organellit | 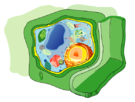 | ||||
| soluseinän |
| ||||
Kasvisolujen jakautuminen |
| ||||
